在我们以前的帖子中,我们集中在轴承相关的各种文章中。如何了解轴承数量。今天,我们将开始与完美天然气的状态方程进行讨论。
博伊尔的法律
气体具有各种重要的性质或变量,如压力,体积,质量和温度。这些气体的变量彼此相关,并且这些变量或性质的大小将确定气体状态。
根据Robert Boyle的说法,在恒定温度下固定质量气体的体积和压力之间会有一种关系。
根据Robert Boyle的说法,在恒定温度和固定质量的气体中,气体的绝对压力将与气体体积成反比。
如果气体的绝对压强是P,气体的体积是V,在恒定的温度下,气体的质量是固定的,我们将会得到绝对压强P和体积V之间的关系
它也可以定义为压力和体积的乘积对于固定质量和恒定温度的气体将是恒定的。
以上关系被指定为博伊尔的法律,因为它由罗伯特博伊尔提供。
让我们用一个例子来了解博伊尔的法律
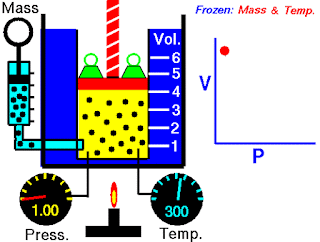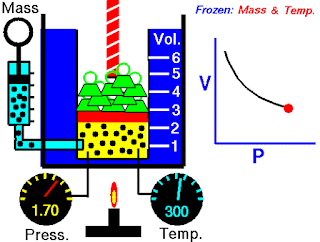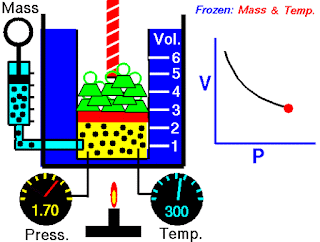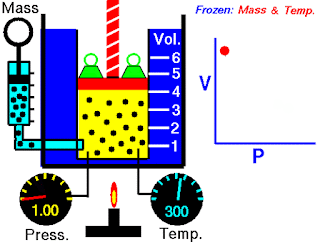
让我们在罐中包含一个气体,并且如图所示,在顶部提供活塞。
允许开始气体有压力1巴和5 m 3。现在我们正在增加活塞顶部的负荷,以增加压力,同时保持温度和气体恒定的质量。
开始时,PV = 5 BAR-M3
随着我们增加压力,气体量开始减少。当压力变为1.5巴时,体积减少到3.333 m3。
在最终状态下,PV = 5 BAR-M3
或者
PV =常数,
Robert Boyle已经拍摄了常量的变量
- 气体温度
- 瓦斯
图片礼貌:谷歌
你有建议吗?请提供您的建议
我们将继续讨论一个完美的天然气的另一种状态方程。查尔斯法律
还讨论














没意见:
发表评论