在我们之前的帖子中,我们集中讨论了一个完美气体的状态方程。波义耳氏定律.今天我们将从另一个理想气体状态方程开始讨论,即查尔斯定律。
查理定律
气体有各种重要的性质或变量,如压力、体积、质量和温度。气体的这些变量是相互关联的,这些变量或性质的大小将决定气体的状态。
查尔斯·吕萨克和盖·吕萨克的科学家们,通过保持气体的质量和压力不变,研究了气体的体积和温度之间的关系。
查尔斯定律描述了行为描述气体在受热时的膨胀行为或描述气体在冷却时的收缩行为。
根据查理定律,如果在定压下加热任何质量固定的气体,气体体积的变化将与温度成正比。
如果气体的绝对温度是T气体的体积是V,在恒定的压强下,气体的质量是固定的,我们就会得到绝对温度T和体积V之间的关系。
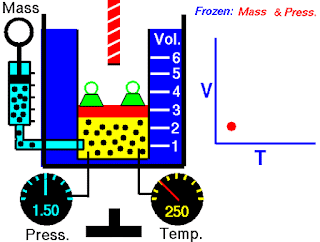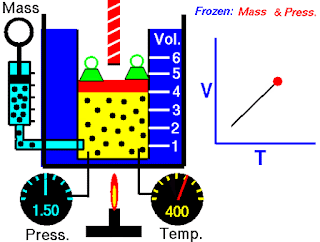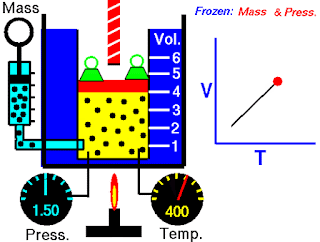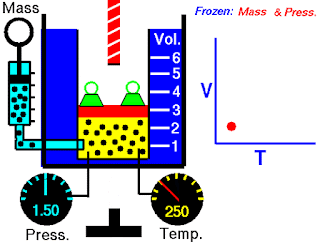
让我们借助下图来了解查尔斯定律
固定质量的气体包含在罐子里,罐子下面有一个提供加热的火炬。通过活塞顶部的螺杆改变活塞的位置,可以改变气体的体积。我们可以看到,体积相对于温度的变化是线性的。
根据查尔斯定律,如果初始状态气体的绝对温度为200 K,体积为5 m3。假设我们把气体加热到400k的温度,那么气体的体积也会增加到10m3。
图片由:谷歌
你有什么建议吗?请提供您的建议
也讨论














没有评论:
发布评论